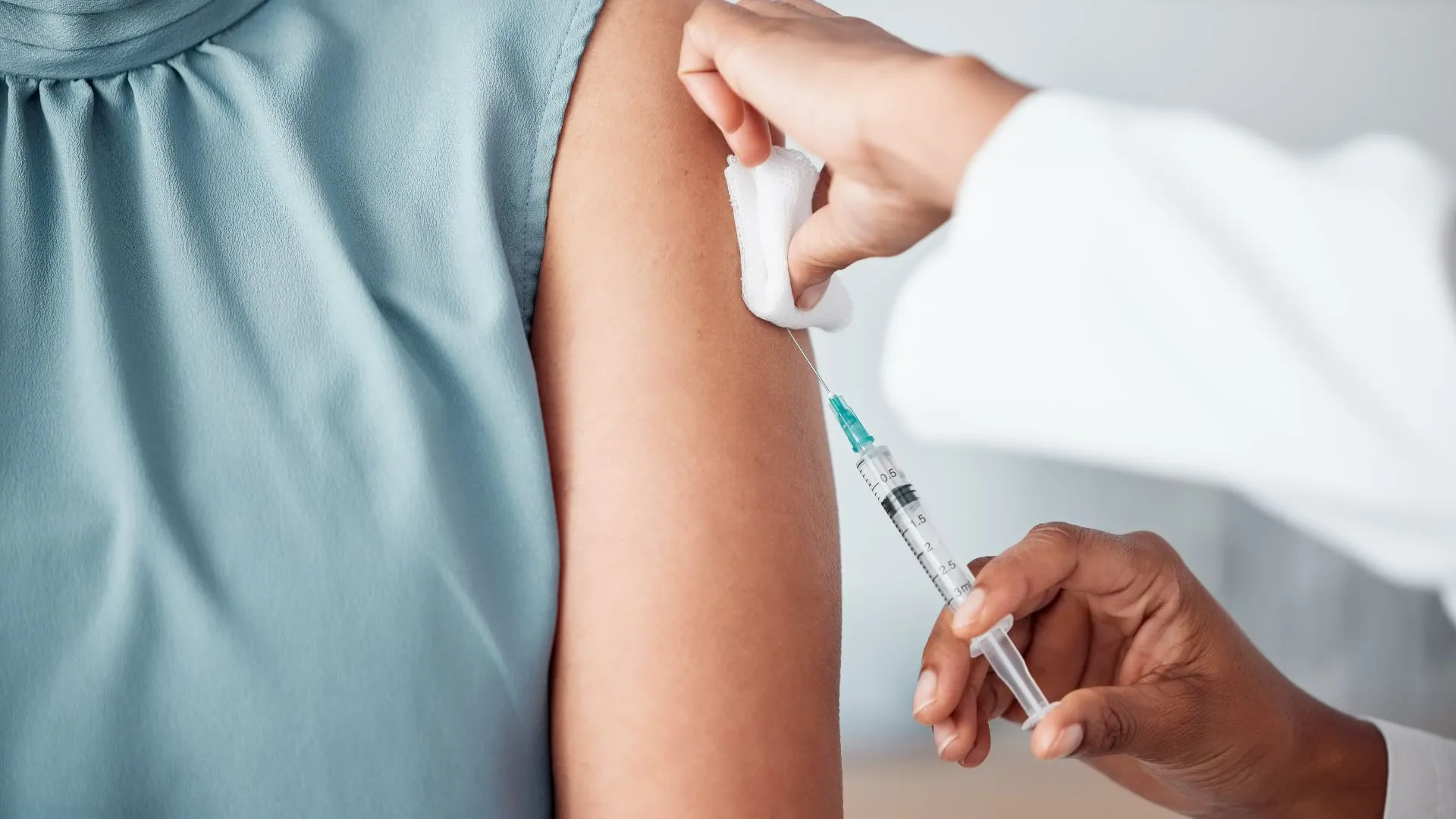
美國已批准全球首款每年兩次的 HIV 預防注射劑,這一里程碑標誌著對抗該病毒的數十年鬥爭邁出了重要一步。
製藥公司 Gilead Sciences 於周三宣布,FDA 已批准 Yeztugo(lenacapavir)用作成人和體重至少 35 公斤的青少年的預防性暴露(PrEP)措施。
儘管全球仍在等待 HIV 疫苗的問世,但許多專家認為這種新的長效選擇可能在預防中發揮重要作用。amfAR(艾滋病研究基金會)公共政策主任 Greg Millett 表示:“這真的有可能結束 HIV 的傳播。”
這種注射藥物預計將成為全球預防努力的關鍵部分,但可及性仍然是一個令人擔憂的問題。
在全球試驗中取得突破性結果
Gilead 的 FDA 批准基於兩項大規模第三階段試驗的數據。在 PURPOSE 1 試驗中,對 5,300 多名位於撒哈拉以南非洲的年輕女性和女孩進行研究,接受 lenacapavir 的參與者中沒有一人感染 HIV。而使用每日藥片的參與者中約有 2% 感染。
第二項研究 PURPOSE 2 對美國及其他高風險國家的同性戀男性和性別多樣者進行了測試。在接受注射的 2,179 人中,僅有兩例感染,成功率達 99.9%。
Gilead Sciences 的董事長兼首席執行官 Daniel O’Day 表示:“今天是對抗 HIV 數十年來的一個歷史性日子。Yeztugo 是我們時代最重要的科學突破之一,提供了一個非常真實的機會來幫助結束 HIV 流行。”
使用便利性可能促進採用
Lenacapavir 以兩次注射的方式施用,注射於腹部皮下,形成一個藥物儲存庫,慢慢在六個月內釋放。這是迄今為止批准的持續時間最長的 PrEP 形式。
與每日藥片或每兩個月一次的注射相比,這種新形式可能對面臨遵從性障礙或擔心污名的人更具吸引力。休斯頓的 Ian Haddock 表示:“現在我忘記我在使用 PrEP,因為我不需要隨身攜帶藥瓶。”他在研究的後續中繼續接受注射。
“無論是男性、女性、同性戀者還是異性戀者,這都擴大了預防的機會,”Haddock 補充道。
健康系統的缺口可能限制可及性
儘管結果強勁,專家們對可及性仍然感到擔憂。對 Medicaid、公眾健康計劃和全球 HIV 資金的削減可能會減緩推廣進程。
Millett 表示:“系統中的巨大漏洞將使我們難以確保不僅能將 lenacapavir 送入人們的體內,還能確保他們能夠回來接受後續劑量。”
目前,美國使用 PrEP 的人數不到五十萬,儘管數百萬人符合資格。
全球可及性計劃正在推進
在美國以外,Gilead 正在歐洲、南非、巴西、加拿大及其他國家尋求監管批准。
該公司承諾向符合條件的無保險美國人免費提供該藥物,並與保險公司合作以擴大可及性。
Yeztugo 僅能預防 HIV,並不保護其他性傳播感染。該公司尚未披露價格。
日本電話卡推介 / 台灣電話卡推介
一㩒即做:香港網速測試 SpeedTest HK
📬 免費訂閱 TechRitual 科技精選
每 3 日由 AI 精選 5 篇最重要香港科技新聞,直送你信箱